El laboratorio farmacéutico Cinfa ha incorporado un doble sistema de seguridad a sus medicamentos para evitar falsificaciones.
De este modo, según informa en un comunicado se anticipa a la hora de disponer todo lo necesario para el cumplimiento de la próxima normativa europea antifalsificación de fármacos, que establece el próximo 9 de febrero de 2019 como fecha límite para su implantación por parte de todas las compañías farmacéuticas.
“La falsificación de medicamentos supone un grave peligro para la salud de las personas, por lo que debemos garantizar su autenticidad antes de ser dispensados al paciente", sostiene su director comercial, José Luis Ergui, quien apunta que la adopción de estas medidas de seguridad y la colaboración de todos los agentes del sector serán "claves para lograrlo”.
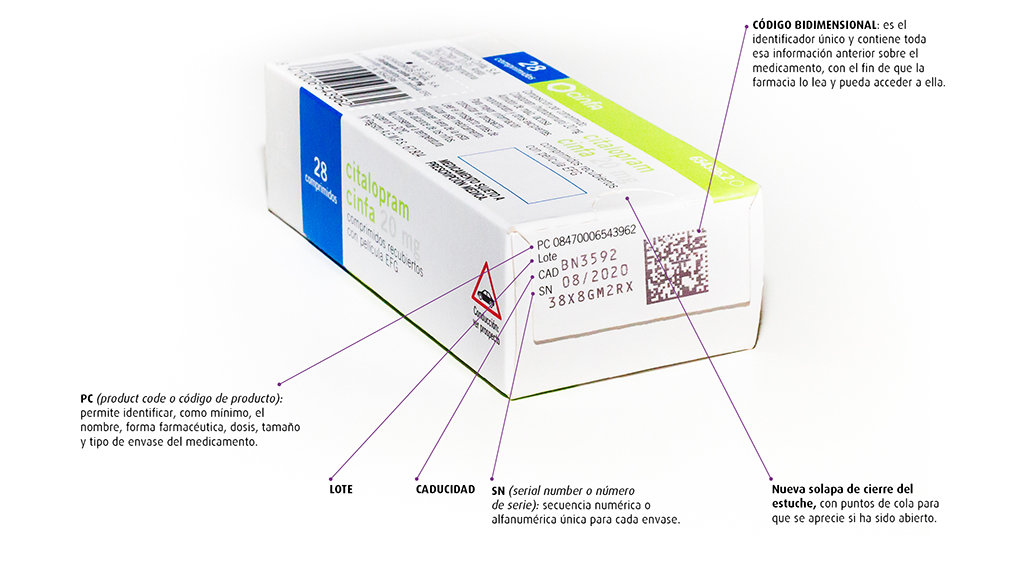
El nuevo sistema de seguridad consta de dos elementos diferenciados, uno de ellos un código datamatrix (código de barras de dos dimensiones) que contiene un número de serie único asignado a cada estuche de medicamento y que permitirá verificar su autenticidad así como su identificación.
Por otro lado cuenta con un mecanismo integrado en el estuche del producto -'tamper evident'en inglés- que, mediante un punto de cola o precinto, asegura que este no haya sido abierto o manipulado.
![]()
Esta normativa, que ya se aplica en países como Estados Unidos, China o India, permitirá que los estados y las compañías farmacéuticas controlen "la legalidad de los medicamentos dispensados”, precisa Ergui.
Para ejecutar este proyecto, que afecta a 800 referencias de medicamentos del laboratorio, Cinfa ha invertido seis millones de euros en adaptar la maquinaria e instalaciones de sus dos plantas de producción ubicadas en Pamplona, y ha necesitado la implicación de una docena de departamentos.
La aplicación de estas medidas de seguridad no solo afecta a las farmacias y a los laboratorios farmacéuticos en Europa, sino también a sus proveedores, que deben adaptar sus medios productivos, instalaciones y sistemas para cumplir con la nueva ley, indica el director comercial.
En la adopción de estas medidas de seguridad ha jugado un papel esencial el sistema informático de la compañía, tanto para generar la información de los códigos datamatrix como en su rápida implementación y funcionamiento.
Estos nuevos códigos son emitidos por una plataforma europea (HUB) con objeto de evitar que dos laboratorios diferentes creen el mismo código. Tras su incorporación al producto fabricado y una vez que la farmacia vende ese medicamento, el código debe darse de baja, de tal manera que si existe otro medicamento con ese mismo número de serie se puede detectar rápidamente que es falso, según explican.
Aunque la normativa, y por lo tanto la lectura de estos códigos datamatrix, entrará en vigor en febrero de 2019, Cinfa ya ha comenzado a distribuir medicamentos con este sistema.